Tiếp cận cầu nối động tĩnh mạch trong chạy thận nhân tạo JAMA 2024
📊Tiếp cận cầu nối động tĩnh mạch trong chạy thận nhân tạo: Một đánh giá tổng hợp
Tác giả Charmaine E. Lok và cộng sự [2024]
JAMA. 2024;331(15):1307-1317. doi:10.1001/jama.2024.0535
🪻Tóm tắt:
Vào năm 2021 tại Hoa Kỳ, có 135,972 người mắc bệnh suy thận cần điều trị thay thế thận (trước đây gọi là bệnh thận giai đoạn cuối) và 808,536 người mắc bệnh suy thận phổ biến cần điều trị thay thế thận.
Trên toàn cầu, phổ biến nhất của hình thức trị liệu thay thế thận là lọc máu (78%), với 22% bệnh nhân còn lại sống nhờ ghép thận.
Khoảng 90% bệnh nhân chạy thận nhân tạo được điều trị bằng chạy thận nhân tạo, và họ cần tiếp cận mạch máu để thiết lập kết nối giữa tuần hoàn mạch máu và máy chạy thận nhân tạo.
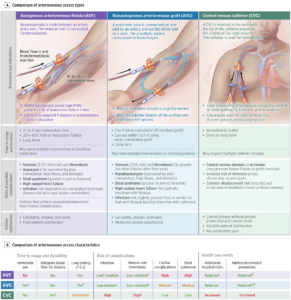
Hai loại đường tiếp cận mạch máu chính là đường tiếp cận cầu nối động tĩnh mạch FAV và ống thông tĩnh mạch trung tâm (CVC).
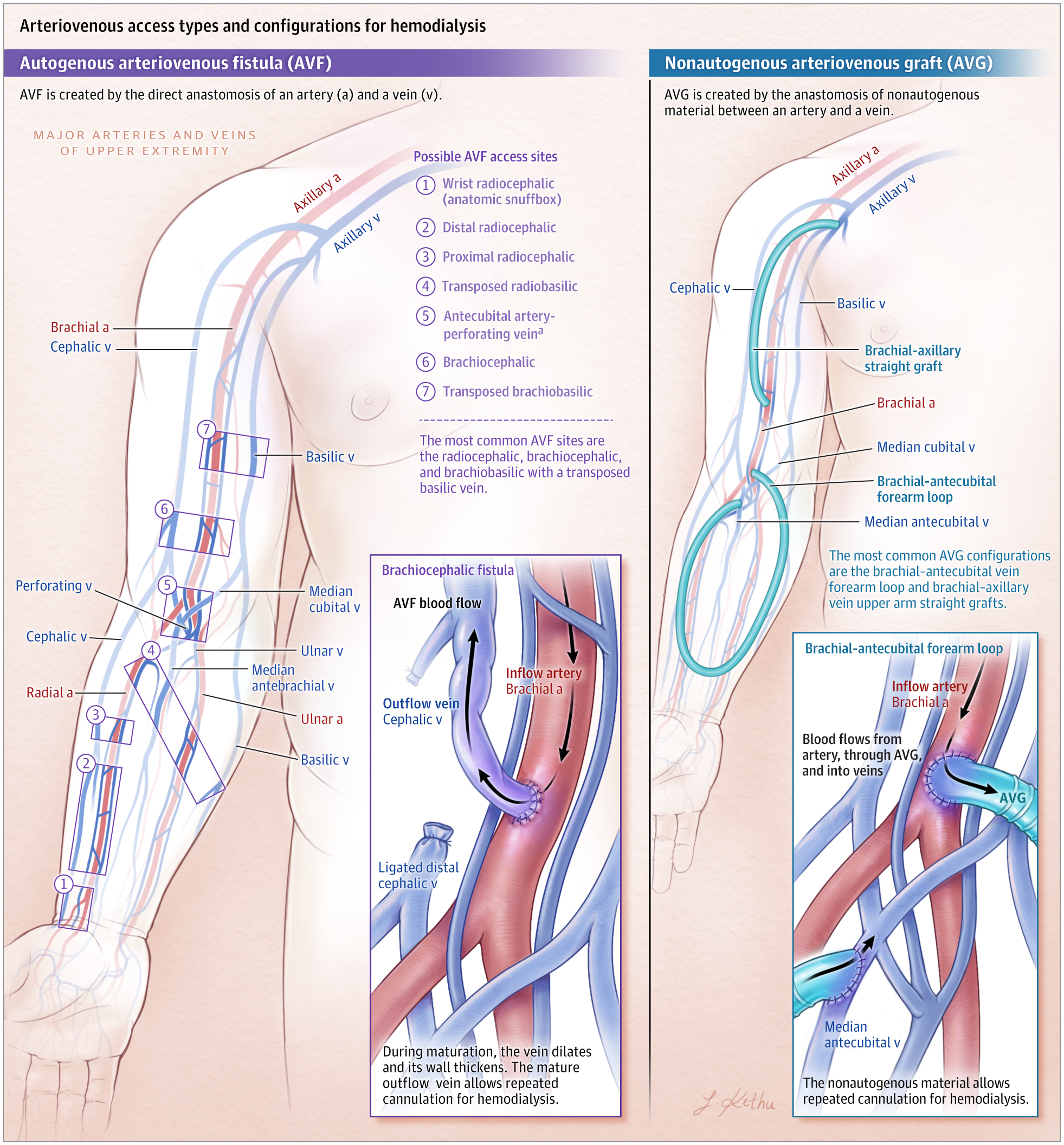
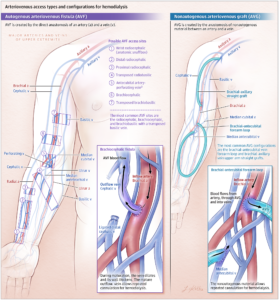
Đánh giá này sẽ tập trung vào đường vào động tĩnh mạch, bao gồm bất kỳ ống dẫn nào được tạo ra liên quan đến nối trực tiếp hoặc gián tiếp giữa động mạch và tĩnh mạch để chạy thận nhân tạo. Cụ thể, đường vào động tĩnh mạch sẽ đề cập đến cầu nối động tĩnh mạch tự sinh (AVF) được tạo ra bằng cách kết nối trực tiếp giữa động mạch và tĩnh mạch, hoặc ghép động tĩnh mạch (AVG), trong đó vật liệu không tự thân được đặt giữa động mạch và tĩnh mạch, được tiếp cận để chạy thận nhân tạo (Hình 1).
Chúng tôi nhấn mạnh thông tin quan trọng nhất đối với các bác sĩ lâm sàng đa khoa, những người hợp tác với bác sĩ thận và bác sĩ can thiệp, điều trị cho bệnh nhân mắc bệnh thận mãn tính.
🍀Quan sát:
📌Tất cả bệnh nhân bị suy thận nên có chiến lược cá nhân hóa (được biết như là Kế hoạch duy trì cuộc sống của bệnh nhân, hoặc Nhu cầu tiếp cận hoặc KẾ HOẠCH) để tiếp cận liệu pháp thay thế thận và lọc máu, bao gồm cả kế hoạch dự phòng cho trường hợp không thể tiếp cận.
📌Bệnh nhân nên được giới thiệu để chạy thận nhân tạo khi tốc độ lọc cầu thận ước tính của họ giảm dần xuống 15 đến 20 mL/phút, hoặc khi việc lọc màng bụng, ghép thận hoặc khả năng tiếp cận mạch máu hiện tại của họ không thành công.
📌Bệnh nhân mắc bệnh thận mãn tính nên hạn chế hoặc tránh các thủ thuật mạch máu có thể làm phức tạp việc tiếp cận động tĩnh mạch trong tương lai, chẳng hạn như lấy máu tĩnh mạch trước khuỷu tay hoặc đặt PICC ở các vị trí dự kiến.
📌Các FAV tự sinh cần từ 3 đến 6 tháng để trưởng thành, trong khi các mảnh ghép động tĩnh mạch tiêu chuẩn có thể được sử dụng từ 2 đến 4 tuần sau khi được thiết lập và các mảnh ghép “ống thông sớm” có thể được sử dụng trong vòng 24 đến 72 giờ sau khi kiến tạo.
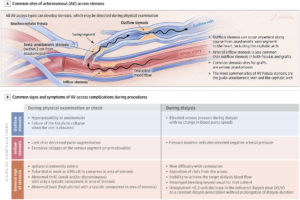
📌Tổn thương bệnh lý chính của các biến chứng liên quan đến dòng chảy của đường vào động tĩnh mạch là tăng sản nội mạc trong đường vào động tĩnh mạch có thể dẫn đến
⚠️hẹp đường vào, hư/giảm chức năng FAV (33%-62% sau 6 tháng)
⚠️hoặc kém lưu thông (60%-63% sau 2 năm)⚠️và lọc máu dưới mức tối ưu.
📌Các biến chứng không thuộc dòng chảy như
⚠️thiếu máu cục bộ bàn tay liên quan đến đường vào (“hội chứng ăn cắp máu”; 1% -8% bệnh nhân)
⚠️và nhiễm trùng đường vào động tĩnh mạch cần được xác định và điều trị kịp thời.
📌FAV và AVG bị nhiễm trùng với tỷ lệ lần lượt là 0,26 ca nhiễm trên 100 bệnh nhân-tháng và 0,39 ca nhiễm trùng trên 100 bệnh nhân-tháng;
📌Nhiễm trùng FAV thường liên quan đến sai sót trong các quy trình kiểm soát nhiễm trùng hoặc không tuân thủ kỹ thuật đặt vô trùng. Nhiễm trùng có thể dao động từ nhiễm trùng cục bộ gần vị trí đặt ống thông cho đến ảnh hưởng toàn bộ đường vào động tĩnh mạch, bao gồm cả chỗ nối.
📌Tỷ lệ nhiễm trùng trong 1 tháng cao hơn ở những bệnh nhân mắc AVG71 (1,8 ca nhiễm/1000 ngày tiếp cận bệnh nhân) so với AVF (1,0 ca nhiễm/1000 ngày tiếp cận bệnh nhân); tỷ lệ nhiễm khuẩn huyết trong 1 năm là tương tự nhau (AVG so với AVF, 0,39/1000 ngày tiếp cận bệnh nhân so với 0,37/1000 ngày tiếp cận bệnh nhân.
⚠️Mạng lưới An toàn Y tế Quốc gia (NHSN), nơi thu thập và phân tích dữ liệu về các bệnh nhiễm trùng liên quan đến lọc máu được báo cáo bởi hơn 6000 cơ sở chạy thận nhân tạo ngoại trú ở Hoa Kỳ, đã phát hiện ra rằng việc đặt ống thông bằng kỹ thuật ‘button hole’ có liên quan đến nguy cơ nhiễm trùng máu liên quan đến đường tiếp cận cao hơn đáng kể (tỷ lệ rủi ro được điều chỉnh, 2,6; 95% CI, 2,4-2,8) và nhiễm trùng tại chỗ tại chỗ (tỷ lệ rủi ro đã điều chỉnh, 1,5; 95% CI, 1,4-1,6) so với đặt ống thông theo nấc thang ‘rope ladder’.
3 thử nghiệm cho thấy không có sự khác biệt về mức độ đau hoặc mức độ hài lòng chung của bệnh nhân giữa các kỹ thuật. Vi khuẩn phổ biến nhất liên quan đến nhiễm khuẩn huyết liên quan đến lỗ khuyết là Staphylococcus Aureus (>50%).
📌Một RCT đã báo cáo rằng vi khuẩn tụ cầu vàng thường gặp hơn ở ‘button hole’ (13%) so với ‘rope ladder’ (0%) sau 1 năm (tỷ lệ tỷ lệ sự cố, 63,3; 95% CI, 22,2-180,0; P< .001).
📌 Việc nhận biết và điều trị kịp thời các bệnh nhiễm trùng AVF và AVG cũng rất quan trọng để tránh làm tổn thương đường vào động tĩnh mạch và lớp da bên trên, có thể dẫn đến xuất huyết ồ ạt.
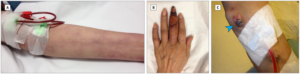
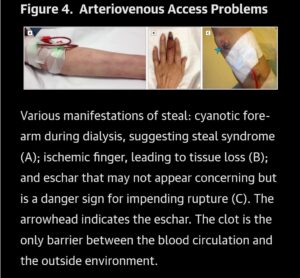
⚠️FAV có nguy cơ xuất huyết cao là một trường hợp ngoại khoa cấp cứu.
🍁Kết luận và tính liên quan
🚩Việc lựa chọn, tạo và duy trì đường nối động tĩnh mạch để tiếp cận mạch máu chạy thận nhân tạo là rất quan trọng đối với bệnh nhân suy thận.
🚩Các bác sĩ lâm sàng đa khoa đóng vai trò quan trọng trong việc bảo vệ khả năng tiếp cận động tĩnh mạch hiện tại và tương lai; xác định các biến chứng tiếp cận động tĩnh mạch như nhiễm trùng, hội chứng thiếu máu bàn tay và suy tim cung lượng cao; và chuyển tuyến kịp thời để tạo điều kiện thuận lợi cho việc tạo đường vào động tĩnh mạch và điều trị các biến chứng đường vào động tĩnh mạch.
❓️Các câu hỏi thường gặp về tiếp cận động tĩnh mạch để chạy thận nhân tạo
🍁Khi nào bệnh nhân nên được chuyển đến can thiệp mạch máu?
Bệnh nhân nên được giới thiệu để đánh giá khả năng tiếp cận mạch máu khi mức lọc cầu thận ước tính (eGFR) là 15-20 mL/phút, bao gồm cả những bệnh nhân đã được ghép thận trước đó.
Tuy nhiên, những bệnh nhân có chức năng thận mức độ thấp ổn định trong nhiều năm cần được theo dõi nhưng có thể không cần tạo đường vào mạch máu. Bệnh nhân đang được thẩm phân phúc mạc nhưng không thành công, cũng như những bệnh nhân đang được thẩm tách máu có đường vào động tĩnh mạch (AV) không có chức năng hoặc hoạt động kém (ví dụ: cần ≥4 biện pháp can thiệp hoặc phẫu thuật khắc phục trong một năm) hoặc có ống thông tĩnh mạch trung tâm nhưng đang đủ điều kiện cho thủ thuật tạo FAV hoặc ghép AV (AVG), cũng nên được giới thiệu đến BS chuyên khoa mạch máu.
🍁Làm thế nào một bác sĩ đa khoa có thể tham gia vào kế hoạch của bệnh nhân?
Các bác sĩ đa khoa nên tích cực tham gia vào chiến lược cá nhân hóa (được gọi là Kế hoạch cuộc sống của bệnh nhân, Nhu cầu tiếp cận [KẾ HOẠCH]) theo 2 cách chính:
(1) kế hoạch cuộc sống của bệnh nhân, bao gồm việc giới thiệu phù hợp đến bác sĩ thận một cách kịp thời để có chỉ định khám lâm sàng và nội thận (tổn thương thận cấp tính hoặc giảm GFR đột ngột kéo dài, bệnh thận mãn tính [CKD] và tăng huyết áp kháng trị với 4 loại thuốc hạ huyết áp trở lên, tiến triển của bệnh thận mạn, sỏi thận tái phát hoặc lan rộng, bệnh thận di truyền, nồng độ kali huyết thanh bất thường dai dẳng, eGFR dưới 30 mL/phút/1,73 m2, albumin niệu đáng kể liên tục [tỷ lệ albumin/creatinine trong nước tiểu > 300 mg/g hoặc 30 mg/mmol] và nước tiểu trụ hồng cầu [RBC] hoặc số lượng hồng cầu lớn hơn 20 trên mỗi trường năng lượng cao được duy trì hoặc không dễ giải thích.
và (2) nhu cầu tiếp cận: vận động và giáo dục bệnh nhân và đồng nghiệp về cách bảo vệ mạch máu nếu bệnh nhân bị bệnh thận mạn hoặc suy thận, chẳng hạn như sử dụng mu bàn tay để tiêm tĩnh mạch và tránh lấy máu/đặt PIVC trước khuỷu tay, đặt ống thông trung tâm ngoại vi, ống thông tĩnh mạch trung tâm, và chọc động mạch quay để đặt ống thông tim, nếu có thể.
🍁Lợi ích của FAV là gì?
Cầu nối FAV đã trưởng thành về mặt chức năng và có thể được sử dụng liên tục bằng 2 kim để thực hiện chạy thận nhân tạo theo chỉ định có tuổi thọ cao hơn và giảm nguy cơ nhiễm trùng so với AVG và ống thông tĩnh mạch trung tâm.